 |
|
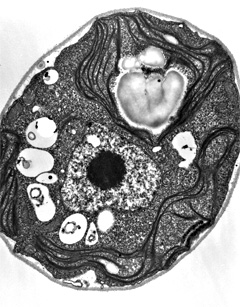
La
micro-algue Chlamydomonas reinhardtii, observée au
microscope électronique. |
C'est ensuite par génie génétique que le Dr.
Yacoby et son équipe ont modifié une micro-algue, plus précisément
Chlamydomonas reinhardtii, afin de modifier le processus de
photosynthèse en détournant certaines de ses fonctions, comme par
exemple la production de sucre, pour augmenter la production
d'hydrogène. Les scientifiques ont ainsi obtenu, en laboratoire, des
micro-algues produisant 400% d'hydrogène de plus que l'algue
d'origine, et ce n'est qu'un début.
L'humanité pourrait entrer dans une nouvelle ère
"Il y a environ 20 000 ans, l’homme a cessé d’être un
chasseur-cueilleur pour se mettre à domestiquer les espèces
végétales trouvées dans la nature et à cultiver lui-même ses
aliments : ce fut la révolution agricole. Mais pour l’énergie, nous
en sommes resté à la collecte de ce que la nature nous fournit, et à
ce jour principalement des combustibles fossiles polluants, qui sont
d’ailleurs en baisse rapide", annonce le Dr. Yacoby.
"Notre découverte constitue une étape importante vers une
nouvelle révolution, qui pourra changer l’avenir de l’humanité : la
production d’énergie propre en quantité suffisante pour répondre à
tous nos besoins. La micro-algue que nous avons créée en laboratoire
possède un potentiel de production de masse de l’hydrogène. Le défi
est maintenant de transmettre ses capacités à des micro-algues d’une
espèce plus durable, capable de vivre dans la nature. En d’autres
termes, l’objectif est de domestiquer des espèces sauvages de
micro-algues, tout comme l’homme a domestiqué pour ses besoins le
blé sauvage. Nous pourrons alors cultiver ces micro-algues
domestiquées, et elle pourront nous fournir de l’hydrogène pour le
carburant des véhicules, et par la suite également pour faire
fonctionner l’industrie", conclut le chercheur.
Les autres participants à l’étude sont le Dr. Oded Liran, le Dr.
Haviva Eilenberg, la doctorante Rinat Semyatich, et l’étudiant de
maitrise Ido Weiner, membres du laboratoire de recherche du Prof.
Yacoby.
Cette étude, publiée ce mois-ci dans les revues Plant Physiology
et Biotechnology for Biofuel (voir références ci-dessous), a
été financée par le département des carburants de remplacement du
bureau du Premier ministre israélien, dirigé par Eyal Rosner.
Jean
Etienne
Sources principales :
The dual effect of a ferredoxin-hydrogenase fusion protein in vivo:
successful divergence of the photosynthetic electron flux towards
hydrogen production and elevated oxygen tolerance (Biotechnology
for Biofuels 20169:182 DOI: 10.1186 / s13068-016-0601-3, publié le
30 août 2016).
Microoxic Niches within the Thylakoid Stroma of Air-Grown
Chlamydomonas reinhardtii Protect [FeFe]-Hydrogenase and Support
Hydrogen Production under Fully Aerobic Environment (Plant
Physiology September 2016 vol. 172 no. 1 264-271 DOI:
10.1104/pp.16.01063).
|